۱٫ معرفی
اخیراً نیتریفیکاسیون همزمان و نیتروژن زدایی اتوتروفیک (SNAD) به عنوان یک جایگزین کارآمد حذف نیتروژن بیولوژیکی به دلیل مساحت کوچک مورد نیاز، ردپای کوچکتر، هزینه انرژی و سرمایه گذاری کمتر و سادگی فرآیند مورد توجه قرار گرفته است. [
۱]. فرآیند SNAD مزیت قابل توجهی نسبت به فرآیند نیتریفیکاسیون و نیتریفیکاسیون جدا شده معمولی دارد. اولاً، فرآیند SNAD عملکرد سریال دو مخزن مجزا را حذف میکند و بنابراین، به روشهای عملیاتی سادهتری نیاز دارد. علاوه بر این، SNAD بازده لجن را تا ۳۰ درصد نسبت به سیستم های حذف بیولوژیکی نیتروژن معمولی (SNR) کاهش می دهد. [
۲].
در طی فرآیند نیتریفیکاسیون اتوتروفیک نیتروژن، نیتروژن آمونیاکی به نیترات و نیتریت اکسید شده و به نیتروژن عنصری کاهش می یابد. در حضور ترکیبات گوگرد معدنی احیا شده، می تواند از آنها به عنوان دهنده الکترون استفاده کند. نیتریفیکاسیون معمولاً به دو مرحله اصلی تقسیم می شود: “نیتریتاسیون” که شامل اکسیداسیون آمونیوم به نیتریت (NH) است.
۴+ → خیر
۲–، و “نیتریفیکاسیون”، که در آن نیتریت بیشتر به نیترات اکسید می شود (NO
2– → خیر
۳–). این مراحل به طور همزمان رخ میدهند و به ترتیب توسط میکروارگانیسمهایی به نام باکتریهای اکسیدکننده آمونیوم (AOB) و باکتریهای اکسیدکننده نیتریت (NOB) انجام میشوند. سپس، نیترات زدایی اتوتروفیک اتفاق می افتد، یک فرآیند بی هوازی شامل کاهش غیر مشابه ترکیبات نیتروژن اکسید شده (NO
2– و/یا خیر
۳–) به عنوان گیرنده های الکترون. در این فرآیند، ترکیبات گوگرد معدنی، مانند گوگرد عنصری (S
0) به عنوان دهنده الکترون عمل می کنند [
۳].
در پساب هایی با نسبت کربن به نیتروژن کم (C/N < 5)، همانطور که در مورد پساب های هاضم های بی هوازی، یا حتی برخی پساب های صنعت، مانند کارخانه های دباغی یا کارخانه های کود،، نیترات زدایی با واسطه میکروارگانیسم های اتوتروف یک روش است. جایگزین جالبی که امکان حذف همزمان اکسیدهای نیتروژن و کاهش ترکیبات غیر آلی گوگرد را بدون نیاز به مکمل با مواد آلی فراهم می کند. [
4]. علاوه بر این، استفاده از میکروارگانیسمهای نیتروژنزدایی اتوتروف نسبت به فرآیند هتروتروف مزایایی دارد: میتواند از مواد معدنی (مانند S
0 در این مورد) به عنوان اهداکنندگان الکترون، از بین بردن مشکلات احتمالی مرتبط با ضایعات آلی، و افزودن کربن آلی خارجی ضروری نیست، هزینه ها و خطرات عملیاتی را کاهش می دهد و تشکیل دی اکسید کربن را حذف می کند. علاوه بر این، باکتری های نیترات زدایی کننده اتوتروف که گوگرد را اکسید می کنند، اکسید نیتروژن کمتری تولید می کنند (N
2O) یک گاز گلخانه ای است [
۱].
ترکیب فرآیندهایی مانند نیتریفیکاسیون و نیترات زدایی اتوتروفیک در یک راکتور منفرد، که در آن جمعیت ها با هم زندگی می کنند و به فرآیندهای همزمان دست می یابند، می تواند منجر به کاهش هزینه های سرمایه گذاری و عملیاتی شود. زیرا نیاز به پیکربندی مقرونبهصرفهتر تصفیهخانههای فاضلاب، دائماً چالشهای جدیدی مانند کاهش لجن باقیمانده، به حداقل رساندن ردپای کربن و کاهش حجم راکتورهای مورد استفاده را به همراه دارد. [
۵,
۶].
شایان ذکر است که مقالات در مورد نیتریفیکاسیون و نیترات زدایی اتوتروفیک گزارش می دهند. با این حال، مطالعاتی در مورد این موضوع مورد نیاز است که در نیتریفیکاسیون اتوتروفیک که در یک راکتور منفرد به طور همزمان با نیتریفیکاسیون و با استفاده از گوگرد عنصری به عنوان دهنده الکترون انجام می شود، بررسی شود. این نشان دهنده یک تازگی در تحقیق چنین فرآیندهایی است.
با توجه به این ویژگی های متوالی فرآیند SNAD، راکتور دسته ای متوالی (SBR) یک انتخاب جذاب است. SBR یک گزینه خوب و جایگزین مناسب به ویژه برای واحدهای صنعتی در مقیاس کوچک تا متوسط است. نتایج عالی برای حذف آلاینده ها با استفاده از این فناوری در کشورهای پیشرفته در مقایسه با سیستم های جریان پیوسته مشاهده شده است. فرآیند اصلی در SBR شامل یک فاز توالی مانند پر کردن، واکنش، ته نشینی و رسم در یک راکتور منفرد است. راکتور در حالت دسته ای با هوادهی و نشست لجن در یک مخزن کار می کند. درمان را می توان در یک حوضه یا حوضه های متعدد انجام داد، که امکان اندازه کوچکتر مخزن و فضاها را فراهم می کند. این سیستم می تواند به طور همزمان کربن آلی، آمونیاک، نیتروژن و فسفر را در یک مخزن با حالت پر کردن و کشش با تغییر شرایط عملیاتی از هوازی به بی اکسیژن و بالعکس تصفیه کند. [
۷,
۸].
با توجه به بررسی مطالعات قبلی، هیچ مطالعه ای در مورد فرآیند نیتریفیکاسیون-اتوتروفیک توالی یابی با استفاده از S انجام نشده است.۰ به عنوان دهنده الکترون جنبه هایی مانند نرخ بارگذاری نیتروژن (NLR) و سینتیک ناشناخته هستند. بنابراین، هدف از این تحقیق توسعه یک فرآیند نیتریفیکاسیون-اتوتروفیک نیتریفیکاسیون با استفاده از S0 به عنوان یک دهنده الکترون در یک SBR منفرد، به بررسی اثر افزایش NLR بر روی فرآیند عملکرد میپردازد. علاوه بر این، پارامترهای جنبشی فرآیند در سیستم SNAD-SBR از طریق آزمایشهای زیستی نیتریفیکاسیون و نیترات زدایی نیز مورد ارزیابی قرار گرفت.
۲٫ مواد و روشها
۲٫۱٫ تلقیح، فاضلاب مصنوعی و راه اندازی آزمایشی
دو نوع تلقیح استفاده شد: اول، لجن بی هوازی از یک تالاب بی هوازی مسدود شده درمان دوغاب خوک به عنوان منبع نیترات زدایی زیست توده استفاده شد. غلظت جامد معلق فرار (VSS) این لجن ۵۳٫۴۷ (گرم VSS/L) بود. دوم، لجن هوازی گرفته شده از تالاب سرپوشیده یک کارخانه کشتار مرغ به عنوان تلقیح نیتریفیک کننده استفاده شد که غلظت VSS 1.8 (گرم VSS/L) داشت.
ترکیب فاضلاب مصنوعی بر اساس استوکیومتری مورد استفاده توسط نویسندگان ویزمن توسعه یافته است. [
۹] و دربی و ویرآقاوان [
۱۰]. علاوه بر این، بر اساس آزمایشهای کونیگ و لیو، ردپایی از عناصر دیگر (ریز مغذیها) به خوراک نیتراتزدایی اضافه شد. [
۱۱]و عناصر دیگر برای خوراک نیتریفیکاسیون استفاده شد [
۱۲]. یک محلول بافر فسفات (K
2HPO
4-KH
2بعد از
۴) برای کنترل pH استفاده شد. برای هر بستر مصنوعی، اسید هیدروکلریک (HCl) یا هیدروکسید سدیم (NaOH) اضافه شد به طوری که PH خوراک در ابتدای چرخه بین ۷٫۰ تا ۷٫۳ بود.
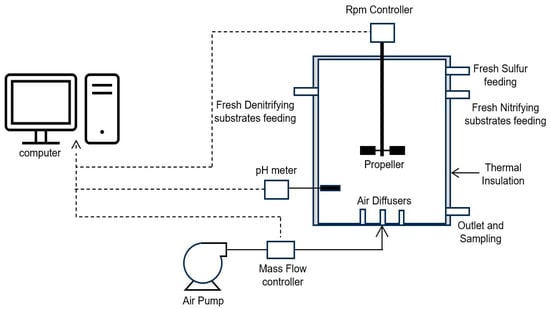
برای آزمایشات آزمایشگاهی از یک راکتور اکریلیک شفاف با پوشش و همزن مکانیکی استفاده شد. این راکتور حداکثر حجم موثر ۳ لیتر داشت.
شکل ۱) دارای سه مجرای ورودی (۱، ۲ و ۳)، یک مجرای خروجی (۵)، و یک مجرای که امکان نمونه برداری و اندازه گیری pH داخل راکتور را فراهم می کند (۴). همچنین دارای یک سیستم هوادهی متشکل از سه پخش کننده هوا (۷، ۸ و ۹) و یک همزن مکانیکی (۶) بود. راکتور با ۱ لیتر از مخلوط لجن هوازی/بی هوازی با نرخ ۳۰/۷۰ تلقیح شد، تخمینی بر اساس تحقیقات Guerrero و همکاران. [
۱۳]. در نهایت، غلظت اولیه زیست توده تقریباً ۹ بود [g/L] (لازم به ذکر است که این زیست توده حاوی انواع میکروارگانیسم ها از جمله هتروتروف بود که به مرور زمان به دلیل عدم وجود بستر آلی کاهش می یابد).
بسترها توسط پمپ های پریستالتیک برای زیرلایه های نیتریفیک کننده و نیترات زدایی به راکتور عرضه شدند، در حالی که گوگرد عنصری (S0) که در نیترات زدایی استفاده می شود، در ابتدای هر چرخه اضافه می شود. جریان ۷٫۸ (mL/min) برای خوراک نیتریف کننده و ۳٫۳ (mL/min) برای خوراک نیترات زدایی تنظیم شد. سه دیفیوزر در پایین راکتور برای تامین اکسیژن داخل آن با استفاده از کمپرسورهای هوای آکواریوم نصب شد که جریان هوای ۲٫۹۶ (L/min) را به دست آورد. همزدن توسط یک تیغه دوار نصب شده در بالای راکتور (۱۰) و در ۱۰۰ دور در دقیقه انجام شد.
تایمرهای متصل به هر یک از پمپ ها و هواده ها، اجرای فازهای مختلف را در سیکل کنترل می کردند. تایمرها هر دوره را با توجه به هر مرحله از چرخه SBR فعال می کردند. راکتور در داخل یک قفس حرارتی با استفاده از یک قلم و یک ساختار فلزی نصب شد. داخل محفظه عایق یک Pt-100 قرار داشت که به یک کنترلر در دمای ۱ ± ۳۱ درجه سانتیگراد متصل بود.
۲٫۲٫ طراحی تجربی
عملکرد راکتور بر اساس یک چرخه با زمان ماند هیدرولیکی (HRT) 72 ساعت توزیع شده در ۳ خوراک طراحی شد (یک چرخه از ۳ تغذیه، یعنی سه چرخه فرعی تشکیل شده بود). چرخه با ته نشین شدن پساب تصفیه شده (۴۵ دقیقه) و تخلیه بعدی (۱۵ دقیقه) به پایان رسید. هر چرخه فرعی با یک خوراک مربوط به یک سوم کل ورودی که باید وارد راکتور شود شروع شد و با مراحل واکنش هوازی و بدون اکسیژن ادامه یافت، همانطور که در نشان داده شده است.
میز ۱. زمان برای هر مرحله چرخه بر اساس تجربیات آزمایشگاهی تعریف شد، با توجه به اینکه واکنش آنکسیک نیترات زدایی فاز محدود کننده در چرخه SNAD است. مراحل تغذیه، ته نشینی و تخلیه دوره های بدون تزریق هوا را تشکیل می دهند، بنابراین بدون اکسیژن هستند و به نیترات زدایی کمک می کنند.
در طول راه اندازی تصمیم گرفته شد که به تدریج نرخ بارگیری نیتروژن (NLR) را تا ۲۰٪ در شرایط عملیاتی زیرلایه چرخه قبلی افزایش دهیم. افزایش NLR زمانی اعمال شد که معیارهای پایداری زیر برآورده شد: ۱-حذف بیش از ۵۰ درصد مربوط به مقدار نیتروژن وارد شده به خوراک به اضافه نیتروژنی که در حجم باقیمانده پس از تخلیه چرخه قبلی بود به دست آمد. ۲- در طول چرخه قبلی، pH همیشه بین ۷٫۰ و ۷٫۶ حفظ می شد، به طوری که نیتروژن از دست رفته در تعادل جرم محصول واکنش نیتروژن زدایی بود که نیتروژن اتمسفر را آزاد کرد و نه از حذف آمونیاک. ۳- معیارهای قبلی باید حداقل برای سه دوره برآورده می شد.
دو مرحله عملیاتی وجود داشت: راه اندازی و بهره برداری.
جدول ۲ تمام غلظت های اولیه TAN و NLR ها را نشان می دهد. معیارهای مورد استفاده برای تعیین اینکه کدام مرحله از برنامه ریزی آزمایشی در حال اجرا بود، رفتار رشد میکروبی و عملکرد راکتور مربوط به سازگاری زیست توده در شرایط مختلف تغذیه بود.
راه اندازی شامل دستیابی به سازگاری میکروارگانیسم هایی بود که فرآیندهای همزمان را انجام می دادند. [
۱۴]. نرخ مصرف بستر آنها برای ارزیابی فعالیت میکروارگانیسم ها بر اساس سطوح حذف به دست آمده توسط فرآیند مورد استفاده قرار گرفت. سپس مرحله تغذیه با ترکیب ثابت ادامه یافت. در کل این عملیات، نسبت کربن به نیتروژن (C/N) هم برای خوراک نیتریفیک و هم نیتروژن زدایی در مورد منابع کربن معدنی (HCO) ثابت باقی ماند.
۳–).
برای همه شرایط، ترکیبات زیر در پایان هر سنجش اندازهگیری شدند: نیتروژن آمونیاکی کل (TAN)، نیتریت، نیترات، سولفات، و کل جامدات معلق (TSS).
برای نیتریفیکاسیون، کارایی فرآیند (
راn) در چرخه به عنوان تابعی از مقدار آمونیوم باقی مانده در راکتور و در تخلیه قبلی ته نشین شده تعریف می شود (معادله (۱)):
جایی که مقدار اولیه آمونیوم در چرخه است که به صورت میلی گرم نیتروژن در لیتر (mg N/L) اندازه گیری می شود. (mg N/L) مقدار نهایی آمونیوم در راکتور است.
حذف کل نیتروژن در پایان چرخه به میزان کارآمدی میکروارگانیسمهای نیتروژنکننده و نیتروژنزدایی بستگی دارد. مقدار اولیه نیتریت و نیترات، نیتروژن اکسید شده موجود، تابعی از میزان آمونیوم اکسید شده در مرحله نیتریفیکاسیون است. راندمان نیترات زدایی (
راد) را می توان مانند معادلات (۲) و (۳) نوشت:
جایی که مترr، نیتروژن (mg N/L) نیتروژن حذف شده است، مترao، نیتروژن (mg N/L) نیتروژن اکسید شده موجود است و مترفو، نیتروژن (mg N/L) نیتروژن اکسید شده نهایی است که مقدار نیتریت و نیترات در پایان چرخه است. مقدار اولیه نیتریت و نیترات با رابطه (۴) به دست می آید:
مقدار اولیه آمونیوم (مترمن، آمونیوم) آمونیوم اضافه شده در خوراک و باقیمانده را در مرحله قبل در نظر می گیرد.
۲٫۳٫ سنجش جنبشی
۲٫۳٫۱٫ تست های هوازی اکسیداسیون گوگرد عنصری
این آزمایش ها برای تعیین اینکه آیا اکسیداسیون گوگرد محصول نیتریفیکاسیون به تنهایی است یا اینکه تزریق اکسیژن در حین نیتریفیکاسیون باعث تولید سولفات می شود طراحی شده است. برای انجام این کار، آزمایشی انجام شد که در آن ۲ گرم از دانه های گوگرد له شده و سپس در یک بشر به ظرفیت ۵۰۰ میلی لیتر آورده شد. قرص های گوگرد عنصری دارای نسبت متوسط بین ۰٫۲ تا ۱ میلی متر با غلظت تقریباً ۹۹٪ بودند. سپس از همان سیستم کمپرسور آکواریوم برای هوادهی ظرف با سرعت جریان ۱٫۹۶ (L/min) استفاده شد که دمای سیستم را در ۳۱ درجه سانتیگراد حفظ کرد. غلظت اکسیژن و سولفات محلول در طول زمان اندازه گیری شد تا مشخص شود که آیا اکسیداسیون گوگرد تولید شده توسط اکسیژن تزریق شده به سیستم اتفاق افتاده است یا خیر.
۲٫۳٫۲٫ تست های نیتریفیکاسیون
چهار سنجش زیستی (نیتریفیکاسیون) در غلظت های اولیه مختلف برای تعیین سینتیک میکروارگانیسم های نیتریفیک کننده انجام شد. برای انجام آزمایشها، ۶۰ میلیلیتر از راکتور (با غلظت مشخص VSS) گرفته شد که در یک بشر ۶۰۰ میلیلیتری درجهبندی شد. سپس مقدار مشخصی آمونیاک وارد شد و آزمایش شروع شد.
در طول جارو، راکتورهای نمونه در دمای عملیاتی اصلی سیستم SNAD-SBR 31 درجه سانتیگراد و با جریان هوای ثابت ۱٫۹۶ (L/min) نگهداری شدند. غلظت تمامی ترکیبات نیتروژن دار (آمونیم، نیتریت و نیترات) و غلظت اکسیژن محلول در زمان های مختلف اندازه گیری شد.
چهار آزمایش نیتریفیکاسیون با غلظت های اولیه مختلف آمونیاک انجام شد. یکی در غلظت آمونیوم بالای ۴۰۰٫۸ (mg N/L)، دیگری با غلظت کم آمونیوم ۱۱٫۱ (mg N/L) و دو آزمایش زیستی دیگر در غلظتهای متوسط مشابه آنچه توسط Beristine استفاده شد انجام شد. -کاردوسو و همکاران [
۱۵] از ۵۰٫۰ و ۵۳٫۹ (mg NH
4+/L).
۲٫۳٫۳٫ آزمایشات نیترات زدایی
دو آزمایش نیترات زدایی انجام شد. برای هر آزمایش، حجم ۵۰ میلی لیتری از راکتور SNAD-SBR گرفته شد و ۱:۳ در بشر رقیق شد. سپس، مقدار اولیه KNO3، NH4+و NaHCO3 در مقادیر استوکیومتری، ۱ گرم گوگرد عنصری به شکل قرص و پتاسیم۲HPO4/KH2بعد از۴ (به عنوان محلول بافر) به هر فنجان اضافه شد. قرص های عنصر گوگرد دارای نسبت متوسط بین ۸ تا ۱۰ میلی متر و ضخامت ۱ میلی متر با غلظت تقریباً ۹۹ درصد بودند.
فنجان ها برای حفظ محیط بدون اکسیژن آب بندی شدند و در ۷۰ دور در دقیقه تکان داده شدند. سپس همانند آزمایشهای نیتریفیکاسیون، نمونههای دورهای گرفته شد. در این مورد، pH اندازه گیری شد تا با توجه به شرایط عملیاتی مشابه سیستم SNAD-SBR کنترل شود. علاوه بر این، غلظت نیترات ها و سولفات ها برای هر نمونه اندازه گیری شد تا به طور تجربی رابطه مصرف و تولید بین این دو ترکیب نشان داده شود.
۲٫۴٫ توسعه مدل جنبشی
فرآیند SNAD توسط دو واکنش موازی انجام می شود: نیتریفیکاسیون و نیتریفیکاسیون. سینتیک مربوطه توسط ویژگی های گروه های میکروبی، نرخ رشد و عناصر بازدارنده داده می شود.
نیتریفیکاسیون یک فرآیند تنفسی هوازی است که توسط دو گروه باکتری انجام می شود: اکسیدان های آمونیاک و اکسیدان های نیتریت. نرخ رشد پایین و بازده کم، باکتری های اکسید کننده آمونیاک اتوتروف را مشخص می کند. بنابراین، نیتراسیون به طور کلی مرحله محدود کننده در نیتریفیکاسیون در نظر گرفته می شود [
۱۶].
سینتیک نوع هالدان ساده ترین توصیف را از مهار بستر ارائه می دهد. سینتیک نوع مونود نیز برای مقایسه و تعیین اینکه آیا تفاوت های قابل توجهی وجود دارد در نظر گرفته می شود. ما سینتیک نوع Haldane یا Monod را برای نیتریفیکاسیون زیست توده ها، به عنوان مثال، AOB و NOB در نظر می گیریم. مهار یک بستر بر اساس سینتیک هالدان، همراه با تابع سوئیچ، با رابطه (۵) توضیح داده شده است. [
۹]:
تابع سوئیچ با این اصطلاح مطابقت دارد
، که در دسترس بودن اکسیژن را توضیح می دهد، که در آن
کاگر مربوط به اکسیداسیون آمونیوم یا نیتریت باشد متفاوت است. برای غلظت های بالای DO (
سی' >>
ک') و برای غلظت ثابت بازداری بالا یا غلظت سوبسترا کم (K
من >> NH
4+، معادله شکل معمولی سینتیک نوع مونود را به خود می گیرد (معادله (۶)) [
۹]:
برای نیترات زدایی، دهنده الکترون گوگرد عنصری است و در دسترس بودن آن در فاز محلول ضروری است زیرا گوگرد عنصری در حلال های قطبی نامحلول است. برای این کار، میکروارگانیسمهای درون راکتور باید موفق به تولید یک بیوفیلم بر روی دانههای گوگرد شوند تا متعاقباً ساختار را از بین ببرند و اجازه دهند گوگرد برای نیترات زدایی اتوتروف در دسترس باشد. [
۱۷]. به این معنا، با استفاده از یک راکتور بستر پر از گوگرد، کونیگ و لیو [
۱۱] نشان داد که یک مدل جنبشی مرتبه متوسط می تواند نیترات زدایی اتوتروفیک توسط بیوفیلم در راکتور را توصیف کند. این به این دلیل است که نفوذ زیرلایه به منافذ بیوفیلم کمتر از اثربخشی کامل است و یک واکنش مرتبه صفر (معادله (۷)) در بیوفیلم به یک واکنش درجه متوسط (معادله (۸)) تبدیل میشود. سطح بیوفیلم [
۱۰].
با این حال، ممکن است واکنش مرتبه اول (معادله (۹))، بسته به رفتار بیوفیلم، یا درجه صفر (معادله (۱۰)) باشد، زیرا غلظت بستر بسیار بالا است.
مسئله ریاضی با استفاده از روش رانگ-کوتا عددی مرتبه چهارم با مرحله یکپارچه سازی ۰٫۵/۱۰۰۰ (روز) حل شد.
مدلهای انتخاب شده برای نشان دادن سینتیک میکروارگانیسمهای AOB در مرحله نیتریفیکاسیون مدلهای Monod و Haldane بودند. شبیه سازی با داده های تجربی مقایسه شد. سپس با استفاده از ابزار Excel، پارامترها با استفاده از تکنیک تحلیل عددی بهینهسازی ریاضی حداقل مربعات با تعریف F تنظیم شدند.
۰ به عنوان تابع کمینه سازی (معادله (۱۱)):
مدلی که کمترین خطا و بالاترین ضریب تعیین را داشته باشد به بهترین وجه نشان دهنده میکروارگانیسم های نیترات زدایی خواهد بود.
۲٫۵٫ تجزیه و تحلیل شیمیایی
ترکیبات نیتروژن دار و سولفات های نمونه ها با استفاده از اسپکتروفتومتر اندازه گیری شد. تمام روش ها از APHA استخراج شد [
۱۸]. برای نیترات ها، اندازه گیری در ۲۲۰ نانومتر به سرعت نیترات را تعیین می کند، زیرا مواد آلی به این بزرگی جذب نمی شوند، و نیترات این کار را در ۲۷۵ نانومتر انجام نمی دهد. اندازه گیری دوم در ۲۷۵ نانومتر مقدار نیترات را تصحیح می کند (روش ۴۵۰۰ NO
3– B روش غربالگری اسپکتروفتومتری فرابنفش). برای نیتریت ها، روش بر پایه تشکیل رنگ آزو بنفش مایل به قرمز است. سیستم رنگ از قانون Lambert-Beer در ۵۴۳ نانومتر پیروی می کند (روش ۴۵۰۰ NO
2– روش رنگ سنجی). برای آمونیاک، روش بر اساس تشکیل یک ترکیب آبی شدید به نام ایندوفنول است که متناسب با مقدار آمونیاک موجود در نمونه است. اندازه گیری اسپکتروفتومتری در ۶۳۵ نانومتر (روش ۴۵۰۰ NH) انجام می شود
۳– روش فنات (F)).
یون سولفات در یک محیط اسیدی با کلرید باریم رسوب می کند و کریستال های سولفات باریم را با اندازه یکنواخت تشکیل می دهد. مقدار آن متناسب با غلظت سولفات های موجود در نمونه و جذب نور سوسپانسیون است. می توان آن را به روش اسپکتروفتومتری در ۴۲۰ نانومتر اندازه گیری کرد (روش ۴۵۰۰ SO42- (ه) روش کدورت سنجی).
کل مواد جامد معلق با استفاده از APHA تعیین شد [
۱۸] (روش ۲۵۴۰).